Les lipoprotéines de basse densité représentent un élément crucial du transport des lipides dans notre organisme. Souvent désignées sous l’acronyme LDL, elles jouent un rôle fondamental dans l’acheminement du cholestérol vers les cellules, mais peuvent également devenir problématiques lorsque leur concentration augmente. Comprendre leur fonctionnement s’avère essentiel pour appréhender les mécanismes cardiovasculaires et optimiser sa santé.
Qu’est-ce qu’une lipoprotéine de basse densité ?
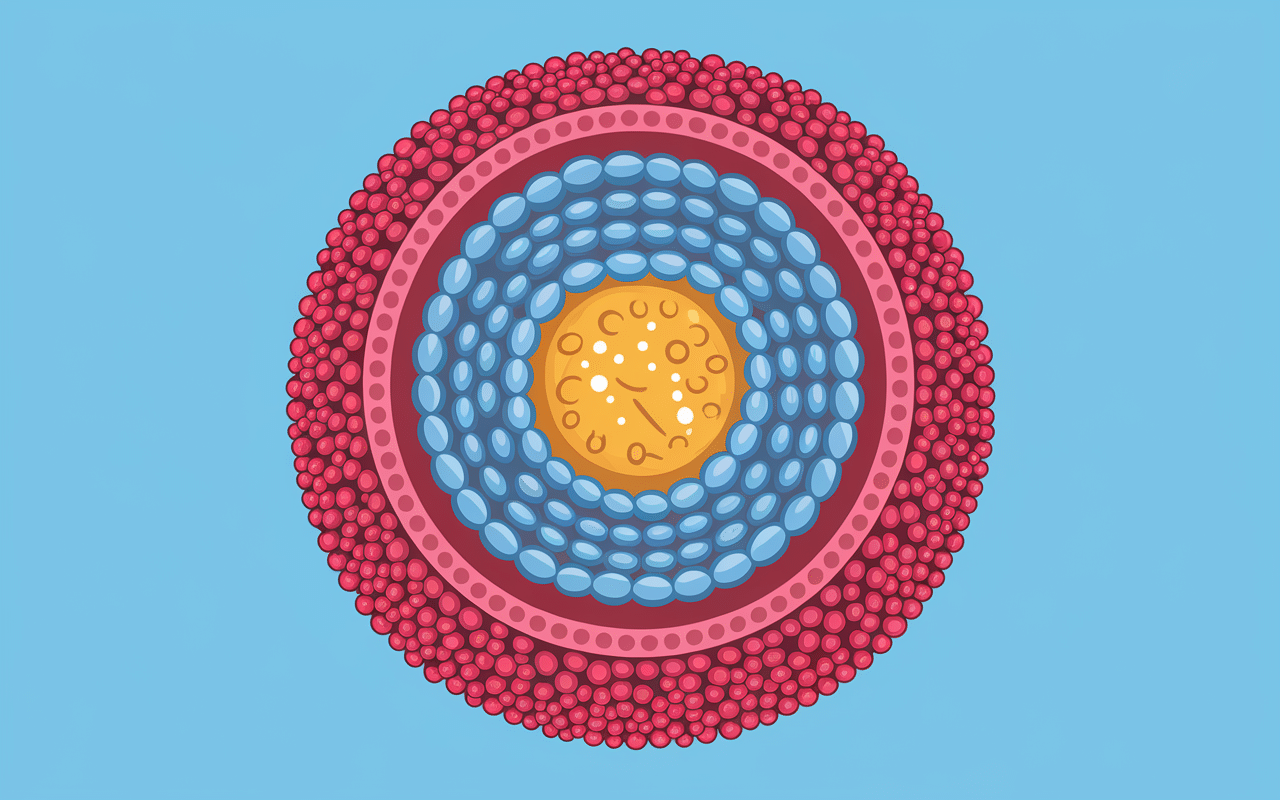
Une lipoprotéine de basse densité constitue une particule complexe composée de lipides et de protéines, spécifiquement conçue pour transporter le cholestérol dans la circulation sanguine. Sa structure sophistiquée comprend un noyau central riche en esters de cholestérol et en triglycérides, entouré d’une monocouche de phospholipides et de cholestérol libre.
L’élément protéique caractéristique des LDL est l’apolipoprotéine B-100, une protéine massive qui enveloppe la particule et lui confère ses propriétés fonctionnelles. Cette apoprotéine joue un rôle déterminant dans la reconnaissance et la captation des LDL par les cellules cibles.
Les caractéristiques physiques des lipoprotéines de basse densité les distinguent nettement des autres particules lipidiques :
| Type de lipoprotéine | Densité (g/mL) | Diamètre (nm) | Fonction principale |
|---|---|---|---|
| VLDL | 0,95-1,006 | 30-80 | Transport des triglycérides |
| LDL | 1,019-1,063 | 18-25 | Transport du cholestérol |
| HDL | 1,063-1,210 | 5-12 | Transport retour du cholestérol |
Formation et métabolisme des lipoprotéines de basse densité
Le processus de formation des lipoprotéines de basse densité débute dans le foie par la synthèse des VLDL (very low-density lipoproteins). Ces précurseurs riches en triglycérides subissent une transformation progressive dans la circulation sanguine grâce à l’action de la lipoprotéine lipase.
Cette enzyme hydrolyse les triglycérides contenus dans les VLDL, libérant des acides gras pour les tissus périphériques. Au fur et à mesure de cette dégradation, les particules VLDL perdent en volume et gagnent en densité, donnant naissance aux LDL. Ce mécanisme de maturation représente la voie principale de production des lipoprotéines de basse densité.
Mécanisme de captation cellulaire
La captation des LDL par les cellules s’effectue via un processus hautement spécialisé impliquant les récepteurs LDL découverts par Brown et Goldstein. Ces récepteurs reconnaissent spécifiquement l’apolipoprotéine B-100 et déclenchent l’endocytose de la particule entière.
Une fois internalisées, les lipoprotéines de basse densité sont dirigées vers les lysosomes où elles subissent une dégradation complète. Le cholestérol libéré peut alors être utilisé pour la synthèse membranaire, la production d’hormones stéroïdiennes ou stocké sous forme d’esters de cholestérol.
Rôle pathologique des LDL dans l’athérosclérose
Lorsque les concentrations de lipoprotéines de basse densité deviennent excessives, ces particules peuvent s’infiltrer dans la paroi artérielle et déclencher un processus inflammatoire complexe. Cette accumulation marque le début de l’athérosclérose, une pathologie progressive qui peut compromettre la fonction cardiovasculaire.
Les LDL piégées dans l’espace sous-endothélial subissent diverses modifications, notamment l’oxydation. Ces lipoprotéines de basse densité oxydées deviennent particulièrement toxiques pour les cellules vasculaires et déclenchent le recrutement de macrophages qui tentent de les éliminer.
Formation des plaques d’athérome
Les macrophages transformés en cellules spumeuses par l’ingestion massive de LDL oxydées constituent le cœur des plaques d’athérome. Ces lésions évoluent progressivement, incorporant du cholestérol, des débris cellulaires et du tissu fibreux.
Certains sous-types de lipoprotéines de basse densité, notamment les LDL petites et denses, présentent un pouvoir athérogène particulièrement élevé. Leur petite taille facilite leur pénétration artérielle, tandis que leur densité élevée favorise leur rétention dans la paroi vasculaire.
Anomalies des lipoprotéines de basse densité et pathologies
Plusieurs pathologies peuvent affecter le métabolisme des lipoprotéines de basse densité, with des conséquences variables sur le risque cardiovasculaire. L’hypercholestérolémie familiale représente l’exemple le plus emblématique de ces dysfonctionnements génétiques.
Cette maladie héréditaire résulte de mutations affectant les récepteurs LDL, l’apolipoprotéine B-100 ou d’autres protéines impliquées dans le métabolisme lipidique. Les patients présentent des concentrations très élevées de lipoprotéines de basse densité dès l’enfance, nécessitant une prise en charge thérapeutique précoce.
Diagnostic et surveillance biologique
Le dosage des LDL constitue un élément central du bilan lipidique. Cette mesure peut être obtenue par calcul (formule de Friedewald) ou par dosage direct, selon les circonstances cliniques. Les valeurs de référence varient en fonction du risque cardiovasculaire individuel :
- Risque faible : LDL < 1,6 g/L (4,1 mmol/L)
- Risque modéré : LDL < 1,3 g/L (3,4 mmol/L)
- Risque élevé : LDL < 1,0 g/L (2,6 mmol/L)
- Risque très élevé : LDL < 0,7 g/L (1,8 mmol/L)
La surveillance régulière permet d’adapter les stratégies thérapeutiques et d’optimiser la prévention cardiovasculaire.
Impact sur la performance et la récupération
La compréhension des lipoprotéines de basse densité s’avère particulièrement pertinente pour les sportifs soucieux d’optimiser leur santé cardiovasculaire. Un métabolisme lipidique équilibré favorise une meilleure oxygénation tissulaire et une récupération optimale après l’effort.
L’activité physique régulière influence positivement le profil des LDL, favorisant la formation de particules plus volumineuses et moins athérogènes. Cette adaptation métabolique contribue à réduire le risque cardiovasculaire tout en améliorant les capacités de performance à long terme.